Gilberto Mora y Obed Vargas lideran convocatoria del Tri Sub-20
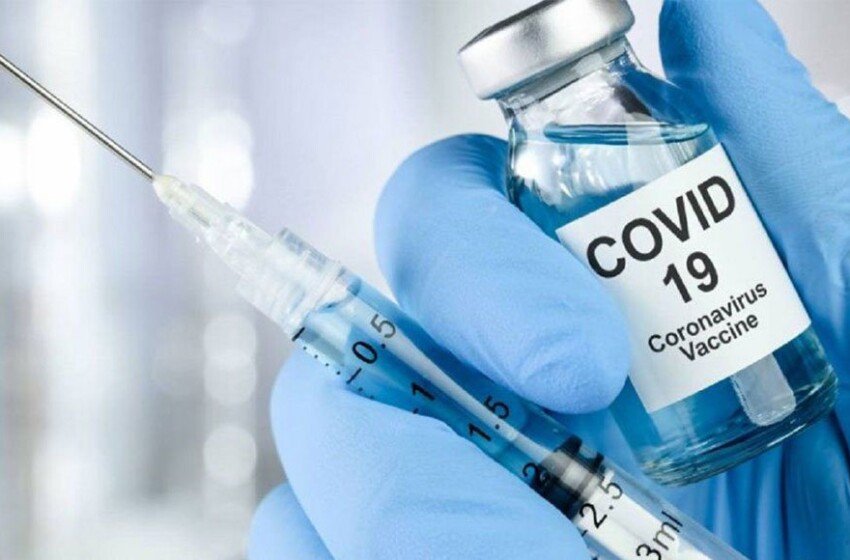
Pfizer solicitará uso de emergencia para su vacuna contra
En una carta abierta publicada el viernes por el presidente y director ejecutivo de Pfizer, Albert Bourla, la compañía farmacéutica anunció que planea solicitar la autorización de uso de emergencia (EUA, por sus siglas en inglés) para su vacuna contra el covid-19 en EE.UU. en noviembre.
«Suponiendo datos positivos, Pfizer solicitará el uso de autorización de emergencia en EE.UU. Poco después de que se logre el hito de seguridad en la tercera semana de noviembre. Todos los datos contenidos en nuestra solicitud de EE.UU. serán revisados no solo por los propios científicos de la FDA, sino también por un panel externo de expertos independientes en una reunión pública convocada por la agencia «, dice la carta.
Sin embargo, Bourla explicó que deben demostrar que la vacuna es un éxito a fin de obtener la aprobación de la Administración de Drogas y Alimentos de EE. UU. para uso público.
«Primero, la vacuna debe demostrar su eficacia, lo que significa que puede ayudar a prevenir la enfermedad covid-19 en al menos la mayoría de los pacientes vacunados. En segundo lugar, e igualmente importante, la vacuna debe demostrar su seguridad, con datos sólidos de seguridad generados a partir de miles de pacientes. Y finalmente, debemos demostrar que la vacuna se puede fabricar de manera constante con los más altos estándares de calidad «, escribió Bourla.
Además, Bourla explicó que la FDA exige que las empresas proporcionen dos meses de datos de seguridad sobre la mitad de los participantes del ensayo después de la dosis final de la vacuna y, en función de su inscripción actual en el ensayo y el ritmo de dosificación, estiman que alcanzarán todos los requisitos para la tercera semana de noviembre, y es posible que sepamos si nuestra vacuna es efectiva o no a fines de octubre.